Quien rehusa escoger la hipotesis como guia debe resignarse a tomar el azar por maestro
Le Bon

CH2 = CH - CH2 - S(O) -S- CH2 - CH = CH2
Este tipo de compuestos donde el azufre de un disulfuro está unido a un oxígeno (sulfóxido) se conoce actualmente como tiosulfinatos (Barton , 1979).
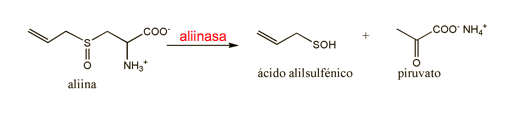
La síntesis natural de la alicina, un compuesto inestable a temperatura ambiente, constituía un enigma por aquellas fechas. Parecía que el ajo solo la producía en determinadas condiciones, por ejemplo, al ser masticado, triturado o simplemente cortado. La respuesta a esta cuestión vino en 1947 cuando Stoll y Seebeck (Stoll y Seebeck, 1947) de los laboratorios Sandoz identificaron la aliina (alil cisteina sulfóxido) ; esta sustancia, presente en el citosol, es el substrato de la enzima aliinasa1 que se encuentra en vacuolas separadas. Cuando el ajo es machacado, las vacuolas conteniendo el enzima se rompen y tiene lugar la reacción con la aliina para formar un producto intermedio que condensa para dar la alicina (ver la sección siguiente).
-Quimica de la alicina
La alicina se sintetiza de forma natural en el ajo cuando la enzima aliinasa entra en contacto con el substrato aliina para producir el ácido alilsulfénico

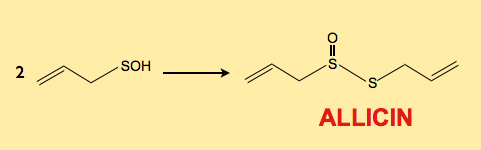
El ácido alil sulfénico condensa para dar la alicina
La alicina puede sintetizarse en el laboratorio por oxidación del disulfuro de dialilo con peróxidos orgánicos, ácido peracético o metacloroperbenzóico. En este trabajo se propone una variante de estas reacciones en la cual el oxidante es transferido de una fase acuosa a otra orgánica mediante una sal de amonio cuaternaria (ver el apartado de síntesis en material y métodos).
Según los primeros estudios de C. Cavallito (Cavallito y Bailey, 1944 ), la alicina es unlíquido oleoso soluble en agua hasta un 2,5% y miscible en alcohol, éter y otros solventes orgánicos como cloroformo, diclorometano o benceno.
La alicina es un compuesto inestable a temperatura ambiente produciéndose en la descomposición reacciones complejas de condensación que veremos mas adelante. Hay dos factores que explican la inestabilidad de la alicina. El primero se debe a la naturaleza de los tiosulfinatos. Estudios comparativos (Block y O´Connor, 1973) del disulfuro de dimetilo y el dimetil tiosulfinato muestran que la unión S-S en el CH3-S-S-CH3 es de 78 kcal/mol, mientras que la del CH3 -S(O)-S- CH3 está unas 29 kcal/mol por debajo. La posible formación de un radical estable RSO., similar al radical peróxido ROO., podría explicar esta relativa debilidad del enlace S-S. Por otra parte, la presencia de dos grupos alilo flanqueando los dos átomos de azufre también contribuye a la inestabilidad de la alicina. Estudios sobre los puntos de ebullición de varios tiosulfinatos (Small y cols, 1947) dieron valores que van desde 20 ºa 30 ºC en nC4H9S(O)SC4H9 hasta 64 ºC en CH3S(O)SCH3. El punto de ebullición de la alicina no se puede obtener pues se decompone al calentarla. Los radicales alilo estables en los productos de descomposición explicarían esta inestabilidad.
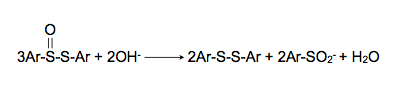
Los tiosulfinatos, se hidrolizan en medio alcalino a disulfuros y sulfinatos (Kice, 1974)
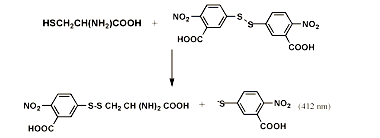
Con los tioles, los tiosulfinatos reaccionan para formar disulfuros. Particularmente interesante es la reacción de la alicina con cisteina
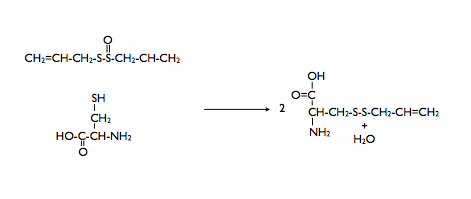
Esta unión con los grupos sulfhidrilo es probablemente la explicación de ciertas propiedades medicinales de la alicina. Enzimas que contengan grupos sulfhidrilo como centro activo podrían bloquearse mediante esta reacción. La alicina, por ejemplo, inactiva la enzima papaína (con centro activo SH). Queda, sin embargo, la pregunta de por qué la alicina –o el extracto de ajo-, no presenta toxicidad en los humanos que la llevan consumiendo durante siglos, dado que las células humanas contienen enzimas de este tipo. Quizá la respuesta esté en la propia química del sistema tiol/disulfuro que es de naturaleza reversible y lábil; así puede ocurrir que después de formado el alil disulfuro, el tiol enzimático se regenere pasado un tiempo por algún reductor presente en el medio (Rabinkov y cols, 1998). Esto explicaría también la acción bacteriostática de la alicina.
La alicina puede formar compuestos de condensación. Los estudios de E. Block (Block, 1985) han develado los mecanismos de estas reacciones. En primer lugar, la alicina se descompone en estas dos especies:
CH2=CH-CH2-SOH ácido alil sulfénico
CH2=CH-CH=S tioacroleína
Después la tioacroleina puede condensar mediante una reacción de Diels-Alder (Block , 1985)
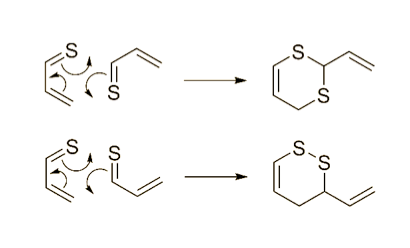
La alicina puede condensar mediante una compleja serie de reacciones para dar los siguientes productos2 (Block y cols,1984)

La formación de estos compuestos depende en gran medida del medio en que esté disuelta la alicina. Los ajoenos y ditiinas se producen con mas facilidad en solventes orgánicos. En agua los productos de descomposición son en su mayoría disulfuros (Iberl y cols, 1990).
Propiedades antibacterianas
Ya en 1944 (Cavallito y Bailey, 1944) se llevaron a cabo los primeros ensayos con alicina en bacterias y hongos. Los resultados mostraron que esta sustancia tenía capacidad inhibitoria sobre bacterias gram positivas y negativas. Frente a Staphylococcus aureus, por ejemplo, mostraba unas capacidad inhibitoria a diluciones de 1/125000 de alicina, que era aproximadamente el 1% de actividad de la recientemente descubierta penicilina. Similares dosis se obtuvieron para Bacillus. paratyphosus y para el Vibrio cholerae3 El crecimiento de las bacterias se reanudaba a las 18 horas de incubación, por lo que la acción era más bien bacteriostática. La comparación con la entonces emergente penicilina, junto a la inestabilidad intrínseca del producto explicarían el escaso interés por parte de la industria en la producción de alicina a gran escala . Se sintetizaron incluso derivados de alicina donde el grupo alilo era substituido por grupos alkilo (Small y cols, 1947) con propiedades antimicrobianas similares a las de la alicina con la ventaja de ser estables a temperatura ambiente. Sin embargo, tampoco se fabricaron compuestos de este tipo con usos medicinales.
Los estudios sistemáticos sobre la alicina como antibiótico han sido sorprendentemente escasos desde aquellas fechas hasta nuestros días. De la bibliografía consultada merece destacarse un estudio sobre los efectos de la alicina sobre la bacteria Salmonella typhimurium por Feldberg y colaboradores (Feldberg y cols,1988). Estos autores describen varias fases en el comportamiento de las bacterias tratadas con alicina: (I) periodo de crecimiento de unos 15 minutos hasta el comienzo de la inhibición, (II) una fase transitoria de inhibición cuya duración depende de la dosis inicial de alicina, (III) una reanudación del crecimiento a una tasa menor que los cultivos sin tratar y (IV) una fase estacionaria con una menor densidad de cultivo. Un descubrimiento significativo fue que la producción de ARN de la bacteria descendió hasta valores por debajo del 1% del valor inicial en los primeros 45 minutos. Luego aumentó hasta alcanzar a las 2 h los valores normales del control. Los autores sugieren un estudio del efecto de la alicina sobre la enzima ARN polimerasa. En todo caso no parece probable que la alicina actúe sobre un único proceso bioquímico, -como sería, por ejemplo, el efecto de la penicilina sobre la formación de la pared bacteriana-. Incluso si suponemos que la alicina actúa solamente sobre enzimas con grupos sulfhidrilo, la variedad de estas enzimas en las bacterias y su total o parcial inactivación provocaría el bloqueo de varios procesos bioquímicos al mismo tiempo de modo que la interpretación final de los resultados es complicada.
A pesar de los inconvenientes citados, la alicina presenta ventajas sobre otros antibióticos que hace que su estudio merezca la atención de los investigadores. Una ventaja es su baja toxicidad. (LD50 de 60 mg/kg en ratón) (Cavallito,1944) y su facilidad de eliminación por la respiración o el sudor. También presenta una gran capacidad de difusión como muestran los estudios con membranas lipídicas(Rabinkov y cols, 1998; Miron y cols, 2000). Además, aunque es bacteriostático, las bacterias no han desarrollado mecanismos de resistencia frente a la alicina como con los otros antibióticos. La acción combinada de la alicina con otros antibióticos al uso es un campo poco conocido pero con interesantes posibilidades.
El efecto antimicrobiano de la alicina sobre el Staphylococcus epidermidis es parte del presente trabajo y se describe en un capítulo aparte (ver la sección de resultados). Tambien se trata por separado la inhibición por la alicina de la producción de biocapas en S. epidermidis, y los análisis del PIA (Polysaccharide Intercellular Ahesin), un polisacárido implicado en la adherencia y formacion de agregados bacterianos . Estos efectos de inhibición no habían sido descrito anteriormente hasta la publicación del trabajo por el Dr. Perez Giraldo y el autor de esta tesis (Pérez Giraldo, 2003).
4. Propiedades antifúngicas
Estudios con extractos acuosos de ajo sobre Candida albicans realizados por Barone (Barone, 1977) mostraron capacidad antifúngica en 39 de las 41 cepas de Candida albicans estudiadas a concentraciones de 68 µg/mL de extracto seco . Las otras dos cepas mostraron un crecimiento moderado. Por otro lado, este autor encontró un incremento en la forma micelial en estos hongos cuando eran tratados con el extracto de ajo. Por su parte Yamada y Azuma (1977) afirman que la alicina es muy efectiva frente a especies de Candida, Cryptococcus, Trichophyton, Epidermophyton y Microsporum a bajas concentraciones, situándose la Concentración Mínima Inhibitoria (CMI) entre 1,57 y 6,25 µg/mL).
5. Propiedades antiparasitarias
El efecto antiparasitario del ajo se conoce desde culturas muy antiguas, y existen referencias históricas de tratamiento frente a disentería y gusanos intestinales (Ankri y Mirelman, 1999). Incluso se ha determinado que a bajas concentraciones (5 µg/mL), la alicina disminuye en un 90% la virulencia de trofozoitos de Entamoeba histolytica (Ankri y cols., 1997).
Merecen destacarse en este apartado los estudios recientes (Coppi y cols., 2006) del efecto de la alicina sobre el plasmodio, causante de la malaria. Esta enfermedad está muy difundida en el mundo y se estima que cada año se diagnostican entre 300 y 500 millones de nuevos casos, de los cuales 1,5 millones son mortales. El plasmodio está cubierto de una proteína conocida como circunsporozita que es procesada por una enzima proteolítica conteniendo grupos sulfhidrilo. Los estudios realizados por el citado grupo muestran que ratones inyectados con esporozitos previamente tratados con alicina no contraen la enfermedad. Además la citada proteasa es responsable de la degradación de la hemoglobina, por lo que su inactivación por la alicina redujo los efectos nocivos,la patogenicidad, del plasmodio en los ratones ya infectados, alargando su supervivencia en 10 días.
Propiedades antitrombóticas
La alicina y alguno de sus productos de condensación como los ajoenos tienen propiedades antitrombóticas (Mayeux y cols, 1988) La alicina inhibe la agregación de plaquetas, además produce vasodilatación de manera similar a los agentes que bloquean el aporte de calcio a las plaquetas, por lo cual estos autores recomiendan los extractos de ajo (con alicina) para prevenir la hipertensión y el infarto.
Derivados de la alicina
Aunque no se estudian en este trabajo, conviene mencionar los productos de condensación de la alicina como E y Z ajoenos porque su formación es espontánea en solventes orgánicos y su obtención relativamente fácil. Además estos compuestos son estables a temperatura ambiente.
La química de estos productos no es tan conocida como la de la alicina5 y su modo de acción antibacteriano no ha sido establecido hasta la fecha; sin embargo, algunos autores (Naganawa y cols, 1996) muestran que los ajoenos son activos frente a bacterias grampositivas con valores de CMI (Concentracion Minima Inhibitoria) del mismo orden de magnitud que la alicina. Para Candida albicans dan un valor de 13 µg/mL, mientras que para las bacterias gramnegativas se requieren dosis por encima de los 100 µg/ mL (como sucede con la alicina)
Al igual que la alicina, los ajoenos han mostrado también propiedades antitrombóticas (Apitz-Castro y cols,1983)
º Magnesiomonoperoxiftálico (Fluka)Procedimiento
ºBisulfato de tetrabutilamonio (Fluka)
ºDiclorometano (Fluka)
ºDisulfuro de dialilo (Fluka)
º Hexano (Panreac)
º Isopropanol (Sigma)
Material
º Silicagel PF 254 indicador fluorescente (Merck) preparada en el departamento de Química Orgánica , Facultad de Ciencias de la Universidad de Extremadura (UEX).
º RMN: Bruker AC-P 200, Facultad de Farmacia de Sevilla.
ºRMN: Bruker AM400, Facultad de Ciencias de la UEX.
º Espectrómetro de masas: Autospec-Q (Micromass), Facultad de Farmacia de Sevilla
ºEspectrómetro de infrarrojo: Jasco- IR 410 (Facultad de Farmacia de Sevilla) y Perkin Elmer 399 (Facultad de Ciencias de la UEX)

Figura 1 a dosificador

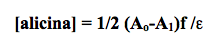
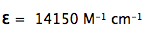

El exceso de cisteína se valora con el reactivo de Ellman
Optimización de la síntesis.
Al final de cada síntesis se tomaba una muestra de la fase orgánica (300 µL), se disolvía en 400 µL de acetonitrilo y se inyectaba en el cromatógrafo: Fase móvil acetonitrilo/ metanol/agua (35/5/60) a 1 mL min-1. Detección, 254 nm (ver la sección de resultados)
Estudio de la transferencia de fase.
Para conocer el proceso de transferencia del oxidante desde la fase acuosa superior a la inferior de diclorometano se midió la variacion del potencial redox en la fase acuosa durante la síntesis. La transferencia de oxidante a la fase orgánica se evidenciaba por la disminucion del potencial de oxidación en la faseacuosa. Se utilizó un electrodo indicador de platino (Metrohm) y uno de referencia Ag/AgCl (Metrohm). El montaje se muestra en la figura 2

Figura 2. Montaje para el seguimiento del potencial redox en la fase acuosa durante la síntesis de alicina : a) electrodo de referencia, b) electrodo de platino c guia, d) varilla de vidrio, e ) agitador de teflón , f) base de teflón, g) barra magnetica h) pH metro, g) ordenador conectado a la salida RS 232
Los valores de potencial se pasaron a un ordenador Apple Macintosh mediante un puerto de serie. Un programa en MS BASIC tomaba los datos y los guardaba en fichero de texto. Los datos se trataron con una hoja de calculo Excel
Análisis del oxidante MMPP
Reactivos
MMPP: Fluka
Sodio sulfito PA: Panreac
Material
PH metro: Orion 720
Electrodo de platino: Metrohm
Electrodo de referencia Ag/AgCl: Metrohm
Colector de datos analógico digital (data logger interface): Vernier Lab Pro
Computadora de mano: Palm Zire 71
Procedimiento
Las titulaciones redox se hicieron con un electrodo de platino y un electrodo de referencia Ag/AgCl . Los electrodos se conectaron a un pHmetro con salida analógica conectada a un colector de datos Vernier Lab Pro unido a una computadora de mano ( PDA) con el programa Data Pro (Vernier software) (ver figura). Los datos de volumen se ingresaron manualmente en la PDA y luego se pasaron a un ordenador de sobremesa. Los datos se trataron con una hoja de cálculo Excel. Las valoraciones se hicieron inmediatamente después de cada síntesis

Figura 3. Sistema de recogida de datos durante la valoración redox
Análisis del periodato.
![]()
A las fracciones cromatográficas (60 gotas/tubo, 1,5 mL) se añadió 1 mL deNaIO4 0,02M (Fluka), se puso un control de 1,5 mL de agua destilada con la misma cantidad de periodato. Los tubos se guardaron en la estufa a 30º . A las 12h se tomó una alícuota de 100 µL y se enrasó en un matraz de 5 mL (dilución 1/50)
Antes del análisis se preparó una solucion del complejo tripiridil triazina (TPTZ)2Fe++ (Pilch,1977) : 75 mg de TPTZ (Fluka) se disolvieron en 46 mL de ácido acético glacial. Se añadieron luego 210 mL de acetato de sodio 1 M y 31,4 mg de Fe(NH4)2(SO4)2.6H2O disueltos en 100 mL de H2O a la mezcla anterior de TPTZ y se llevó a 1L Esta solución debería tener un valor de absorbancia de 1,9 apropximadamente. Antes de la determinación se diluyó con solución tampón de AcOH/ AcONa de pH 4,2 hasta un valor de absorbancia entre 0,8 y 0,9. Una alícuota de 3,00 mL se llevó a una cubeta espectrofotométrica de 1cm de paso de luz. Esta solucion es la que se valoró con la muestra. Con una micropipeta se añadieron volúmenes fijos (20 a 40 µL ). Despues de cada adición la mezcla se homogeneizó con otra micropipeta de 1 mL (ajustada a 450 µL) hasta obtener un valor de absorbancia estable. Se hicieron entre 6 y 8 mediciones por muestra. Los fundamentos del método se describen a continuación.
Consideramos las adiciones sucesivas de un oxidante sobre un estandar de volumen inicial Vo Cada adicion hace disminuir la respuesta del aparato de medida (la absorbancia). Inicialmente suponemos una estequiometría 1:1. Tambien suponemos que la reaccion es irreversible7
Si a un volumen Vo de reactivo se le añaden volumenes Vi de muestra, la variación de la absorbancia sería
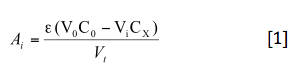

Por lo que el valor final Cf sería
Cf = 1/2 f Cx [2]
Siendo f el factor de dilución (50 en nuestro caso).
Estimacion del error.
Como el valor de Cx se obtiene de la pendiente m , el error cometido es:
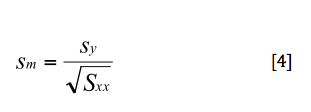
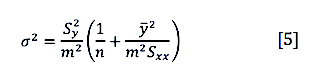
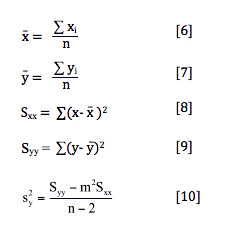
siendo n los grados de libertad (número de puntos).
En el cálculo de las diferencias con el control se siguió el procedimiento usual de propagación de errores (Ramis).
IS = DOb/DOc
Siempre se efectuaron estudios control (sin alicina) y todas las determinaciones se realizaron al menos por triplicado y se repetieron al menos tres veces.
En determinadas valoraciones también se empleó el método cualitativo de macrodilución en tubo (Christensen y cols, 1982), tiñendo la superficie interna del vidrio con azul alciano o safranina.
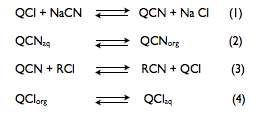
Esquema I
En nuestro caso, el agente de transferencia de fase Q es el catión tetrabutil amonio y el oxidante inicial en fase acuosa es el magnesiomonoperoxiftálico MMPP. La reacción (1) sería la formacion de una sal de amonio cuaternario por el MMPP, que pasaría a la fase orgánica donde está disuelto el (Alil)2 SS produciendose la oxidación para dar la alicina.
Hay dos importantes factores que el químico debería tener en cuenta cuando se planifica este tipo de síntesis. Primero, estudios cinéticos muestran que la constante global de la reacción descrita es proporcional a [Q] (Starks 1973). El segundo factor concierne al paso 4, en el cual parte de la sal permanecerá en la fase orgánica en mayor o menor cantidad según la constante de reparto de la sal. Esta constante también afecta a la constante final de velocidad. Como veremos mas adelante, estas consideraciones y algunas diferencias en las condiciones experimentales8 deberían tenerse en cuenta en la síntesis de la alicina.
Procedimiento experimental
Aunque el método llevó ciertamente a la obtención de la alicina (Cruz, 2001), los rendimientos fueron bajos, por lo que se modificaron las condiciones experimentales para optimizar la síntesis.
Se realizaron tres experiencias para diferentes proporciones R= [Q]/[Ox] (1, 3 y 5), y un ensayo en blanco (R=5) sólo con el oxidante y la sal de amonio cuaternaria. Las reacciones se llevaron a cabo a 18±1 ºC. Con el fin de mejorar la reproducibilidad, las dos fases se agitaron simultáneamente a 170-180 rpm (ver el montaje en material y métodos). Al final se tomó una muestra de la fase acuosa para analizar el oxidante y otra de la fase orgánica que se analizó por HPLC, para calcular el rendimiento.
Se hizo un seguimiento de la transferencia de oxidante a la fase acuosa midiendo la disminución del potencial redox en la fase acuosa con el tiempo (ver Fig.2, en material y métodos). La figura 1 corresponde al ensayo en blanco (R=5), sin disulfuro en la fase orgánica. Se aprecia una pronunciada caída del potencial hasta alrededor de los 6 minutos; luego se produce un descenso más suave hasta el final, (30 minutos). La primera parte puede deberse al transporte a la fase orgánica del oxidante unido al surfactante. La disminución posterior puede resultar por una descomposición del peróxido en la fase acuosa, dado que no hay reacción en la fase orgánica.
La adición de disulfuro de dialilo a la fase orgánica produjo curvas similares a la descrita pero con valores iniciales de potencial más bajos. No sabemos con certeza la causa de este descenso, aunque es posible que la sal de amonio cuaternaria transportase algo del disulfuro de dialilo a la fase acuosa, y esto puede afectar al electrodo de referencia (Ag/AgCl) produciendo valores iniciales de potencial más bajos para valores de [Q] crecientes9 . En todo caso se aprecia un aumento de la pendiente inicial al aumentar el valor de R, lo que sugiere una mayor transferencia inicial para las reacciones con mayor concentración de sal de amonio. Estos resultados cualitativos fueron completados con el análisis cuantitativo del MMPP en la fase acuosa usando el electrodo de Pt como indicador en valoraciones redox, como se describe en el siguiente apartado.

Figura 1. Variación del potencial redox en la fase acuosa, ensayo en blanco.

Figura 2 . Variación del potencial redox para tres ensayos con diferentes valores de R=[Q]/[Ox]
b) Titulación
El oxidante (MMPP) en la fase acuosa se determinó por valoración con un patrón de sulfito sódico 0,05 M. Se hizo un ensayo previo con una solución 0,01 M (valor nominal) de MMPP. En la figura 3 se aprecia claramente el punto de equivalencia en las dos curvas.

Figura 3. Titulación de MMPP inicial (20 mL), y en fase acuosa (50 mL) para R=1 incluyendo la derivada numérica .

de modo que la reacción puede escribirse como:

La valoración de 20 mL de MMPP dio un punto final de Ve = 6,7 mL, que corresponde a una concentración real de 8,4 x 10–3 M, o un 84% de pureza (estaba etiquetado como ~80%, valoración redox). El exceso de oxidante en la fase acuosa al final de la síntesis se determinó de igual modo (ver figura 2). Para una alícuota de 50 mL, el oxidante transferido se calculó como:
[Ox]i = 0.84 [Ox]n
[Ox]t = [Ox]i -1/2Ve (mL) 0.05M/50(mL)
%T = 100.[Ox]t/[Ox] i
Los subíndices i y n se refieren a la concentración inicial (real) y nominal de oxidante. Los valores de Ve y T se dan en la tabla 1. La disminución de oxidante para R1 y R3 difiere sólo un 7%, lo que explica el rendimiento final similar de alicina. En la figura 4 se muestran los cromatogramas de HPLC del medio de reacción después de 30 min. Puede observarse que para R1 = 5 y un exceso de oxidante sobre el disulfuro de 1.5 (tres veces la cantidad estequiométrica) hay una conversión casi total de (Alil)2SS en alicina.
Los resultados muestran que, aunque hay una transferencia de fase, se requiere un considerable exceso de surfactante para transferir el oxidante al medio de reacción, por lo que, estrictamente, no se puede hablar de “catálisis” en este proceso. Debido a la naturaleza inestable de la alicina, la estrategia de síntesis consiste en transferir el oxidante a la fase orgánica lo más rápidamente posible y trabajar a bajas temperaturas (baño de hielo)
Al final de la síntesis,el exceso de oxidante y el producto de reducción, (ftalato de magnesio y otras sales) se eliminan por cristalización en frío; además se han eliminado los pasos de lavado de los extractos que propician la descomposición de la alicina.
Tabla 1. Pérdida de oxidante para varios valores de R=[Q]/[Ox
|
Q, mmol |
Ra |
Veq, mL |
% |
|
1,03 |
1 |
8,46 |
63 |
|
3,09 |
3 |
6,75 |
70 |
|
5,15 |
5 |
5,15 |
77 |
|
5,5 |
5 (blanco) |
14,5 |
36 |
a. Inicial MMPO, 1.03 mmol, diallil disulfuro,1.37 mmol,[Ox]/[Dis] =0.75, o sea, 1.5 veces la cantidad equivalente
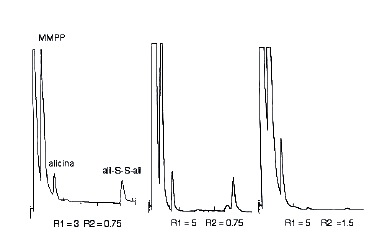
Figura 4. Cromatogramas de la fase orgánica para varios valores de R1 = [Q]/[Ox] y R2 = [Ox]/[disulfuro]. Se aprecia la transferencia de oxidante (MMPP) al medio de reacción
Resultados espectroscópicos.
Espectro de infrarrojo


Figura 1. Espectro de infrarrojo de alicina (Facultad de Farmacia de Sevilla)
Espectros de H RMN
La molécula de alicina con los protones diferenciados es:

El azufre que lleva el oxígeno es tetraédrico y, por tanto, los protones d y e son diferentes (diastereotópicos). El espectro se muestra en la Figura 2
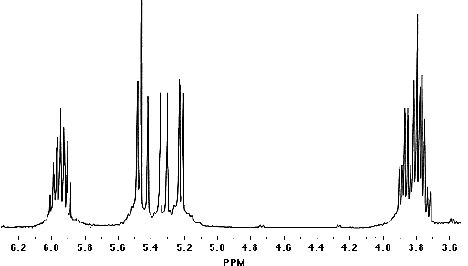
Figura 2. Espectro RMN de la alicina (400MHz, Facultad de Ciencias de Badajoz)
Como puede verse en la figura 2 el espectro es muy complejo y no es fácil la asignación de los picos a los desdoblamientos teóricos.

Figura 3 Espectro COSY de la alicina (200Mz, Facultad de Farmacia de Sevilla)

Figura 4- Espectro DEPT-135. (Facultad de Farmacia de Sevilla)

Figura 5. Espectro de masas de la alicina (Facultad de Farmacia de Sevilla)
Una sorpresa fue que el pico más abundante fuese el M-1 (M/Z = 161), y no el M+1 (M/Z = 163) como cabría esperar de la protonación de la molécula. El catión alílico estable podría originar los picos M/Z 73: [CH2=CH-CH2-S]+ y 75: [CH2=CH-CH2-SH2]+. Una interpretación posible de los picos M/Z 161 , 163 y 145 se ilustra en el esquema siguiente.

El pico de 145 admite otra posibilidad. Debido a que la muestra estuvo bastante tiempo en diclorometano (y por encima de –70ºC,como es aconsejable), pudo haber tenido lugar una condensación de tipo Diels-Alder ya mencionada y dar alguno de estos compuestos (Calvey, Tung, 1994):

ambos con M =144; la protonación daría el pico de 145.
El pico a 235 apoyaría la idea de una condensación durante el periodo de almacenamiento produciéndose los ajoenos (M=234) ya mencionados en la introducción.

El pico a 217 podria deberse a la protonación del oxígeno y posterior eliminación de agua tal como se describió para la alicina .
El pico a 237 podria ser de M+H para 34S con aprox. 14,3% respecto al pico a 235, que se ajusta bastante bien a las abundancias relativas del 4,5% de 34S para tres atomos de azufre (Gross, 2007).

Tabla 1.- Actividad antimicrobiana de alicina sobre 37 cepas de S. epidermidis.
|
CMI (µg/mL) |
|||
|
CMI50 |
CMI90 |
intervalo |
|
|
Resistentes a meticilina (n =18) |
4 |
8 |
<0.25-16 |
|
Sensibles a meticilina |
4 |
8 |
<0.25-16 |
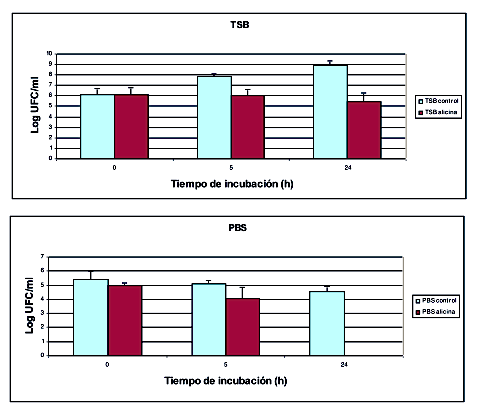
Figura 8.- Actividad de 80µg/mL de alicina (10xCMI) sobre S. epidermidis ATCC 35984 en fase de crecimiento activo sobre TSB y en un sistema de “no crecimiento” sobre PBS estéril.
En la figura 8 representamos la actividad de alicina sobre S. epidermidis ATCC 35984 en fase exponencial de crecimiento. Se observa como en el medio sin alicina (control) las bacterias crecen sin dificultad hasta alcanzar su fase estacionaria, mientras que cuando suplementamos el medio con 80µg/mL de alicina (10 x CMI) el cultivo no crece, produciéndose un descenso suave (8,8%) en las 5 primeras horas. A las 24 h de cultivo el número de bacterias ha descendido un 77,6% con respecto al número inicial de bacterias. Debemos destacar que en este momento aún permanecen viables un número significativo de bacterias (2,75 x 105 UFC/mL). Este efecto bacteriostático de la alicina ya ha sido descrito por otros autores (Feldberg y cols,1988) sobre diferentes bacterias.
Por otro lado analizamos el efecto de alicina sobre bacterias utilizando un sistema de “no crecimiento” (figura 8). En este caso las bacterias, procedentes de una fase estacionaria, se lavaron en PBS estéril para eliminar los restos del medio nutritivo, y se resuspendieron en el mismo PBS. Se le añadió 80µg/mL de alicina (10 x CMI) y se hicieron recuentos de bacterias a diferentes tiempos. Los resultados indican (figura 8) que la alicina provocó un descenso importante en el número de bacterias ya que a las 5 horas habían desaparecido el 91.5% de las bacterias con respecto al control en el mismo tiempo. No se detectaron bacterias viables a las 24 h de incubación.
Como se comentó en la introducción, la explicación generalmente aceptada de la acción antimicrobiana de la alicina se debería a la inhibición de enzimas conteniendo grupos sulfhidrilo en el centro activo (Ankri y Mirelman, 1999). En la bibliografía consultada no aparecen estudios sobre el mecanismo de inhibición de estafilococos por la alicina. Sin embargo, un estudio sobre la síntesis de la pared bacteriana en S. epidermidis durante los años 70, por Wickus y Strominger (1973) puede proporcionar algunas pistas. Estos autores estudiaron la enzima enolpiruvato-UDP-N-acetilglucosamina transferasa en S. epidermidis. Esta enzima incorpora el grupo enolpiruvato a la UDP-N-acetilglucosamina (UDP-NAG) según:
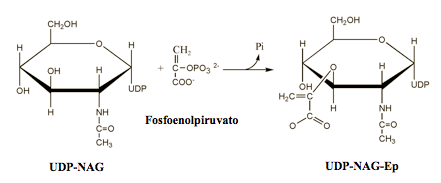
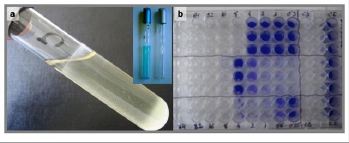
Figura 1 a) formación de biofilm en medio de cultivo sin teñir, y con azul alciano (tubo superior izquierda) b) en microplacas para análisis espectrofotométrico (tinción con violeta cristal)
Inhibicion de biofilm por la alicina
![]()
Durante los ensayos con alicina como inhibidor del crecimiento pudimos observar un efecto adicional sobre la formacíon de biocapas. Cuando se cultivaban cepas de Staphylococcus epidermidis productoras de biofilm en presencia de alicina a concentraciones iguales o incluso por debajo de la CMI, la cantidad de biomaterial adherido a las paredes del tubo de cultivo disminuia de forma considerable. En la figura2 podemos ver como el control (tubo de la derecha) muestra un anillo tipico de biofilm y un fondo blanquecino, mientras que el tubo de la izquierda con alicina a 4 µg/mL presenta una mayor transparencia. Estos resultados cualitativos se completaron con un estudio cuantitativo del biofilm que se detalla en el siguiente apartado.

Figura 2. Fomacion de biofilm en presencia y ausencia de alicina
Los ensayos se hicieron en placa de cultivo siguiendo el método de Christensen con violeta cristal. (ver material y métodos)
Las cepas fueron separadas en dos grupos según su resistencia a la meticilina. Diecinueve cepas eran meticilin susceptibles y las otras 19 eran meticilin resistentes.
En presencia de concentraciones subinhibitorias de alicina se observó una reducción variable en la formación de biofilm (Tabla 1). Después del crecimiento con 1/2 CMI la producción de biofilm fue considerablemente menor en comparación con el control (p= 0.05) con una producción media de 6± 3% (rango de 4 a 10%). A 1/4 y 1/8 de la CMI la producción media de biofilm con respecto al control fue de 12± 5% (rango de 6 a 19%), y 26 ± 17% (rango de 8 a 54%), respectivamente. Para concentraciones menores se observó un comportamiento variable. Dos cepas mostraron una reducción significativa a una concentración de alicina 1/16 de la CMI.
Tabla 1. Indice de slime para varias concentraciones de alicina
|
CEPA |
Control |
1/2 CMI |
1/4 CMI |
1/8 CMI |
1/16 CMI |
1/32 CMI |
|
ATCC35984 |
2,8±0,5 |
0,1±0,1** |
0,2±0,2** |
1±1 |
2,7±0,7 |
2,9±0,5 |
|
2893 |
2,5±0,3 |
0,10±0,05* |
0,2±0,1* |
0,6±0,8 |
1,9±0,6 |
2,2±0,1 |
|
9542 |
1,4±0,5 |
0,1±0,1** |
0,2±0,1 |
0,3±0,3* |
0,5±0,5* |
0,8±0,5 |
|
12 |
1,9±0,5 |
0,08±0,05** |
0,2±0,2* |
0,1±0,1* |
0,2±0,2** |
0,5±0,2 |
|
2526 |
2,9±0,6 |
0,2±0,1* |
0,5±0,4 |
0,7±0,4 |
2±1 |
3,4±0,4 |
El índice de slime se expresa como (DO biofilm/DO cultivo) ± dt
*p = 0,05 ; ** p = 0,01, CMI alicina = 4 µg/mL
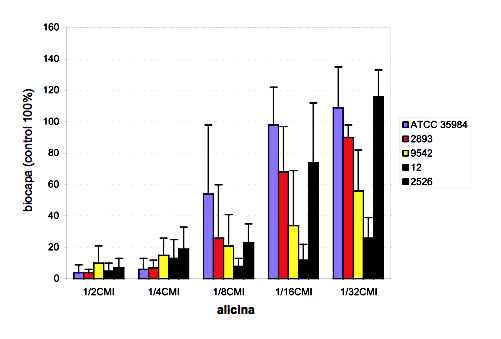
Figura 3 . Índice de slime de las cinco cepas estudiadas para varias diluciones de alicina. CMI = 4 µg/mL
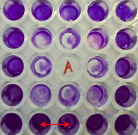
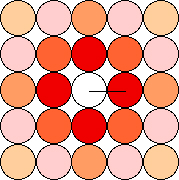
Figura 5. Disposición de los pocillos en en la placa de microtitulación.La distancia entre los centros es 9 mm. A partir de este valor se calcula fácilmente la distancia a los otros pocillos
Tabla 2.Valores promediados de la densidad óptica y el índice slime en los pocillos alrededor del pocillo central con alicina 3mM
| color |
Distanciaa (mm) |
Crecimiento(DO 490nm) |
Biofilm (DO 490nm) |
I. S.b |
| • |
9 |
0,47 ± 0,05 |
0,08 ± 0,02 |
0,17 ± 0,05 |
| • |
12,7 |
0,46 ± 0,05 |
0,51 ± 0,4 |
1,11 ± 0,4 |
| • |
18 |
0,42 ± 0,04 |
1,34 ± 0,4 |
3,19 ± 0,4 |
| • |
20,1 |
0,41 ± 0,03 |
1,45 ± 0,2 |
3,53 ± 0,2 |
| • |
25,4 |
0,45 ± 0,03 |
1,6 ± 0,1 |
3,55 ± 0,1 |
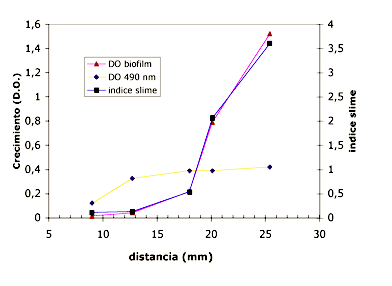
Figura 6. Variación del crecimiento y biofilm con la distancia al pocillo central de alicina
Para confirmar estos resultados se realizaron ensayos similares sustituyendo las bacterias por una solución conteniendo una enzima sensible a la alicina como la papaína. Esta enzima contiene un grupo SH como centro activo y rompe uniones peptídicas, por lo que se incluye dentro de la familia de enzimas proteolíticas. El empleo de una enzima de este tipo nos permite controlar mejor las condiciones experimentales; su concentración puede ser estimada a partir de las referencias comerciales, como su actividad enzimática, y también por análisis específicos como referido ensayo de Ellman. Una posible inhibición de la papaína por los vapores de alicina o algún subproducto derivado de esta debería reflejarse en una pérdida de actividad enzimática cuando se le adiciona un substrato específico como el BAPNA (ver material y métodos). La acción de la papaína sobre esta molécula se ilustra en el esquema siguiente
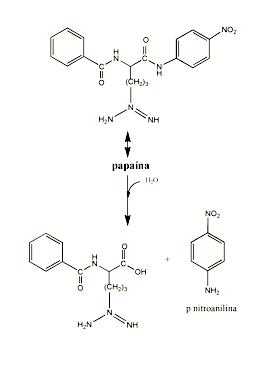
La paranitroanilina que se libera puede seguirse espectrofotométricamente a 405 nm.
Se hizo un ensayo se a temperatura ambiente, dejando las placas durante 1 hora. Se puso enzima en dos pocillos contiguos al que contenía alicina. Una serie de tres pocillos en el extremo de la placa se recubrió con cinta adhesiva para preservarlo de los vapores de alicina y se usó como control.
En la figura se representa la disposición de las soluciones de enzima a lo largo de una columna con los pocillos marcados con las letras A, B ,C
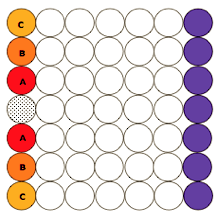
Figura 7. Disposición de las soluciones de enzima, A,B,C con alicina en el pocillo central. En el extremo (marcados en azul) se pusieron los controles sellados.
En la figura 8 se representan los valores promediados de los controles y de los pocillos equidistantes al pocillo central de alicina.
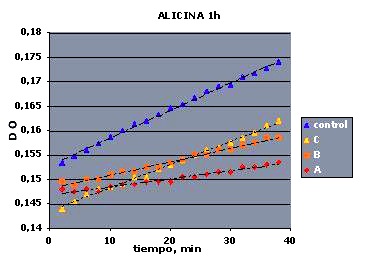
Figura 8. Actividad enzimática promediada en los pocillos control y en la columna con alicina en el pocillo central
En la figura 8. vemos que la pendiente de las series varía según C>B>A, lo que indica una inhibición creciente de la enzima a medida que disminuye la distancia al pocillo central; además, estas tres curvas presentan una pendiente menor que la serie control con los pocillos cubiertos. Estos resultados concuerdan con los obtenidos en los ensayos con bacterias